第五章 化工生产中的重要非金属元素 阶段重点突破练(一)(含答案)—2024春高中化学人教版必修二
2024-01-31 19:24:03 学考宝 作者:佚名
Word文档版
学考宝(xuekaobao.com)友情提示:html格式不完整,如有需要请根据文末提示下载并进行二次校对Word文档。
第五章 化工生产中的重要非金属元素
阶段重点突破练(一)
一、二氧化硫的性质及应用
1.二氧化硫表现还原性的反应是( )
A.SO2+Na2CO3===Na2SO3+CO2
B.SO2+2H2S===2H2O+3S
C.SO2+2NaOH===Na2SO3+H2O
D.SO2+2H2O+Cl2===H2SO4+2HCl
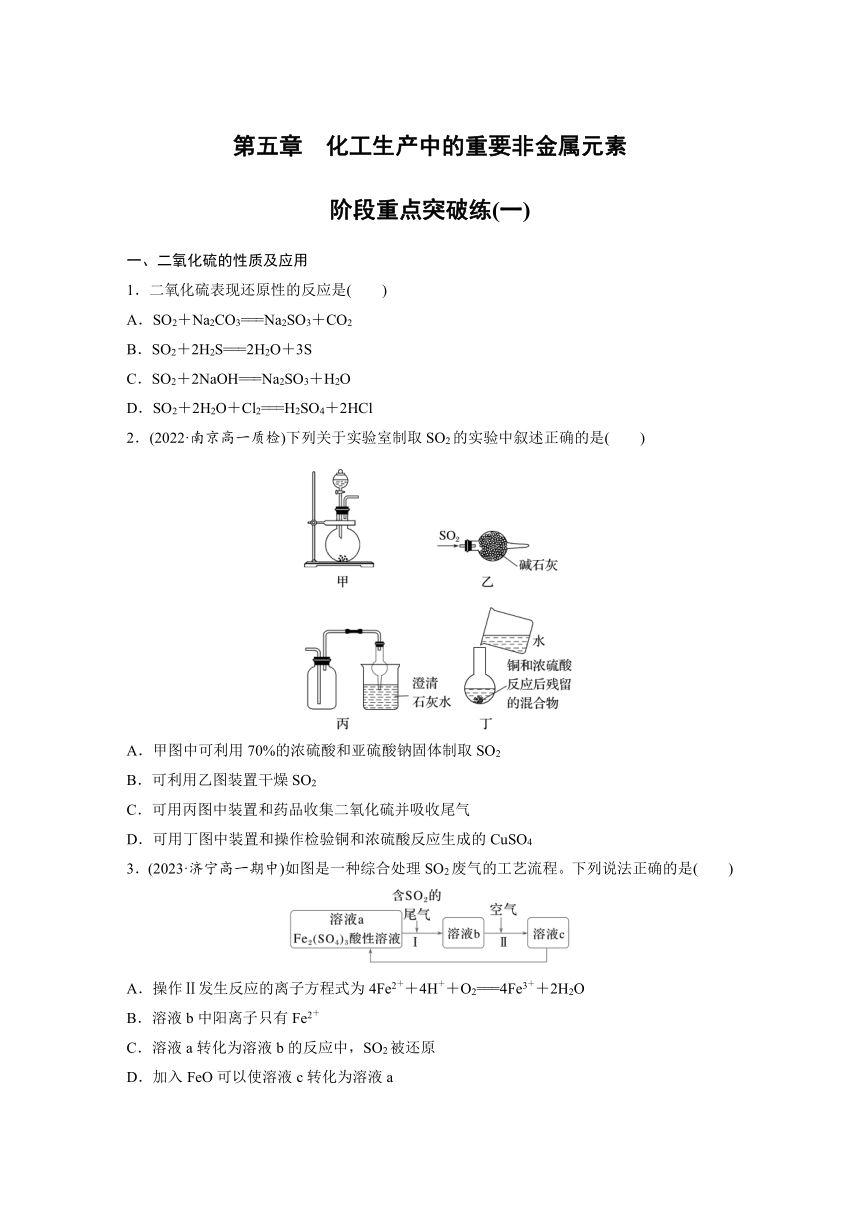
2.(2022·南京高一质检)下列关于实验室制取SO2的实验中叙述正确的是( )
A.甲图中可利用70%的浓硫酸和亚硫酸钠固体制取SO2
B.可利用乙图装置干燥SO2
C.可用丙图中装置和药品收集二氧化硫并吸收尾气
D.可用丁图中装置和操作检验铜和浓硫酸反应生成的CuSO4
3.(2023·济宁高一期中)如图是一种综合处理SO2废气的工艺流程。下列说法正确的是( )
A.操作Ⅱ发生反应的离子方程式为4Fe2++4H++O2===4Fe3++2H2O
B.溶液b中阳离子只有Fe2+
C.溶液a转化为溶液b的反应中,SO2被还原
D.加入FeO可以使溶液c转化为溶液a
4.(2023·青岛高一期中)实验小组研究SO2与Na2O2的反应。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有________性,SO2与Na2O2反应生成Na2SO4。
(2)如用图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导管口,木条复燃。
①A中反应产生SO2的化学方程式是________________________________________________
_______________________________________________________________________________。
②B中的试剂为________________,其主要作用是干燥SO2。
③能证明假设1成立的实验现象是_________________________________________________。
(3)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4。从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的________________________(只写一条)有关。
二、H2SO4的性质及应用
5.(2023·福建莆田高一期中)下列关于浓硫酸和稀硫酸的叙述正确的是( )
A.都具有强氧化性
B.一定条件下都能与铁反应
C.加热时都能与铜反应
D.都能作为气体干燥剂
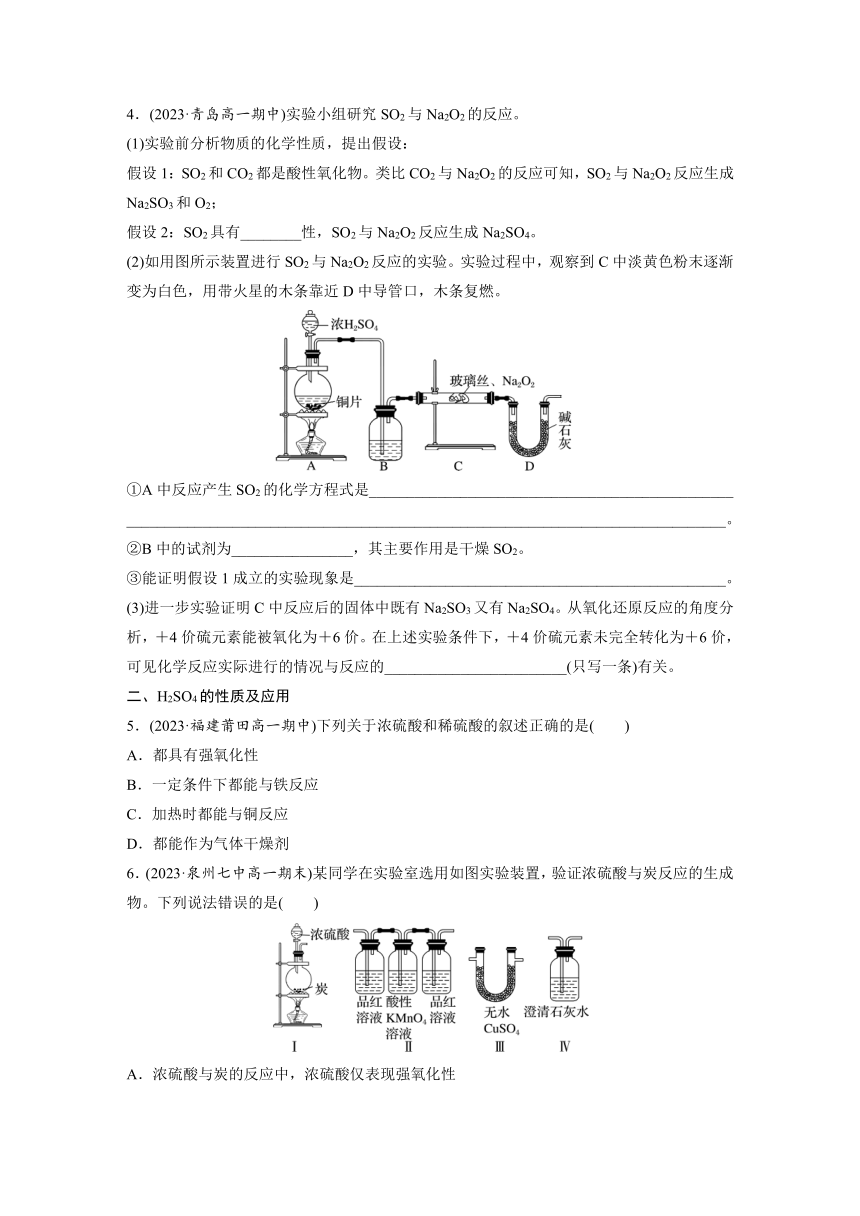
6.(2023·泉州七中高一期末)某同学在实验室选用如图实验装置,验证浓硫酸与炭反应的生成物。下列说法错误的是( )
A.浓硫酸与炭的反应中,浓硫酸仅表现强氧化性
B.验证产物的正确连接顺序为Ⅰ→Ⅲ→Ⅱ→Ⅳ
C.装置Ⅱ中两侧品红溶液在实验设计中的作用不相同
D.若连接顺序为Ⅰ→Ⅱ→Ⅲ→Ⅳ,无法检验产物中有无CO2
7.将3.2 g Cu投入100 mL稀硫酸中加热,没有明显变化,若边加热边缓缓加入一定量H2O2,金属Cu逐渐溶解,则下列说法正确的是( )
A.反应过程中有刺激性气味的气体生成
B.温度越高反应速率越快
C.若Cu和硫酸恰好完全反应,则硫酸的物质的量浓度为0.5 mol·L-1
D.反应中硫酸既表现出酸性又表现出强氧化性
8.某同学在研究Fe与H2SO4的反应时,进行了如下实验。
(1)实验Ⅰ中,铁与稀硫酸反应的离子方程式为_____________________________________。
(2)实验Ⅱ中,铁丝表面迅速变黑,反应很快停止,其原因是____________________________
_______________________________________________________________________________。
(3)实验Ⅲ中,加热后产生大量气体,A试管中溶液的红色褪去,C处始终未检测到可燃性气体。B试管中发生反应的离子方程式是____________________________________________。
(4)对比实验Ⅰ、Ⅱ和Ⅲ,得出以下结论:
①浓硫酸和稀硫酸都具有氧化性,但原因不同。浓硫酸的氧化性源于+6价的硫元素,稀硫酸的氧化性源于_________________________________________________________________。
②造成生成物多样性的主要因素有_________________________________________________。
三、硫酸根离子的检验及应用
9.对于某些离子的检验及结论正确的是( )
A.加稀盐酸有无色气体产生,该气体能使澄清石灰水变浑浊,原溶液中一定有CO
B.加氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液中一定有SO
C.某溶液为蓝色,该溶液中可能含有Cu2+
D.某溶液中加入碳酸钠溶液有白色沉淀生成,则该溶液中一定有Ca2+
10.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,粗盐精制的实验流程如下。下列说法不正确的是( )
A.在第①步中使用玻璃棒搅拌可加速粗盐溶解
B.第⑤步操作是过滤
C.在第②③④⑥步通过加入化学试剂除杂,加入试剂顺序为NaOH溶液→Na2CO3溶液→BaCl2溶液→稀盐酸
D.除去Mg2+的反应的离子方程式为Mg2++2OH-===Mg(OH)2↓
四、含硫物质的性质及其相互转化
11.(2022·山东临沂高一期中)下列说法正确的是( )
①硫的非金属性较强,所以只以化合态存在于自然界中
②分离黑火药中的硝酸钾、木炭、硫黄要用到二硫化碳、水及过滤操作
③硫与金属或非金属反应时均作氧化剂
④硫在过量空气中燃烧产物是SO3
⑤不能由单质直接化合而制得CuS、CuCl2、Fe2S3、FeCl2
⑥因为SO2具有还原性,所以不能用浓硫酸干燥SO2
A.②③ B.② C.②④⑥ D.②⑤
12.(2023·石家庄高一期中)如图是硫元素的常见化合价与部分含硫物质类别的对应关系图,下列说法正确的是( )
A.X、Z都可以被W的浓溶液氧化
B.常温下,Y难溶于水,微溶于酒精,易溶于CS2
C.Z具有漂白性,所以可以使酸性高锰酸钾溶液褪色
D.W的浓溶液使胆矾变白,说明W的浓溶液具有脱水性
13.灼烧绿矾的化学方程式为2FeSO4·7H2OFe2O3+SO2↑+SO3↑+14H2O。将绿矾灼烧后生成的气体通入如图装置,下列叙述不正确的是( )
A.①中棉花球颜色褪去
B.②中棉花球颜色褪去,体现了SO2的还原性
C.③中同时有BaSO3和BaSO4生成
D.④中可发生反应:SO2+2NaOH===Na2SO3+H2O
14.(2023·河北衡水高一月考)硫代硫酸钠晶体(Na2S2O3·5H2O)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分Na2S,含少量Na2SO4 )及纯碱等为原料制备Na2S2O3·5H2O的流程如图:
下列说法正确的是( )
A.Na2S2O3作脱氯剂时主要利用其氧化性
B.“净化”时加入的试剂X可选用BaCl2溶液
C.“反应”过程中体系pH大小对产品产率无影响
D.提纯Na2S2O3·5H2O时,应先用水洗,再用乙醇洗涤
15.某小组同学设计实验实现几种价态硫元素的转化。
Ⅰ:从下列试剂中选择合适的试剂实现S(+6价)→S(+4价)的转化。
试剂清单:①浓H2SO4;②稀H2SO4;③酸性KMnO4溶液;④Na2SO3溶液;⑤Cu;⑥品红溶液。
(1)写出实现转化的化学方程式:___________________________________________________。
(2)设计实验,证明实现了该转化(写出操作和现象):____________________________________
_______________________________________________________________________________。
Ⅱ:实现硫元素在0价、+2价、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2Na2SO3溶液Na2O3溶液X
(3)ⅰ中加入的物质是________,该转化说明SO2的类别是________。
(4)写出ⅲ反应的离子方程式:___________________________________________________。
阶段重点突破练(一)
1.D 2.A 3.A
4.(1)还原 (2)①Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O ②浓硫酸 ③C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导管口,木条复燃 (3)温度(或者条件)
解析 (2)③若假设1成立,则SO2与Na2O2反应生成Na2SO3和O2,根据C中淡黄色粉末变白色说明过氧化钠发生了反应,根据带火星的木条靠近D中导管口,木条复燃,可证明产物有氧气,从而证明假设1成立。(3)在上述实验条件下,+4价硫元素未完全转化为+6价,说明反应不能充分进行,这个反应是在常温条件下进行,温度对物质的性质有一定影响,导致反应不能充分进行。
5.B 6.D 7.C
8.(1)Fe+2H+===Fe2++H2↑ (2)铁丝表面生成致密的氧化膜,阻止反应进一步进行 (3)SO2+2OH-===SO+H2O (4)①+1价的氢元素 ②反应物的浓度、温度
9.C
10.C [加入过量的氢氧化钠可以将镁离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入碳酸钠要放在加入氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为NaOH、BaCl2、Na2CO3或BaCl2、NaOH、Na2CO3等,Na2CO3要在BaCl2的后面加,C错误。]
11.B [硫的非金属性较强,硫元素主要以化合态的形式存在,但自然界中也存在游离态的硫,①错误;硝酸钾易溶于水,木炭难溶于水,S易溶于二硫化碳,故分离黑火药中的硝酸钾、木炭、硫可以先用水溶解后过滤,分离出硝酸钾,再在滤渣中加入二硫化碳,溶解并过滤,实现碳和S的分离,②正确;S为0价,属于中间价态,与金属反应作氧化剂,与非金属单质反应可以作还原剂,③错误;硫在过量空气中燃烧产物是SO2,④错误;不能由单质直接化合而制得CuS、Fe2S3、FeCl2,CuCl2可以由单质化合反应生成,⑤错误;二氧化硫和浓硫酸不反应,能用浓硫酸干燥,⑥错误。]
12.B [在一定条件下浓H2SO4可以氧化H2S,但不能与SO2发生反应,A错误;Y是S单质,在常温下,S难溶于水,微溶于酒精,易溶于CS2,B正确;Z是SO2,SO2具有漂白性,可以使品红溶液褪色,但SO2使酸性高锰酸钾溶液褪色是由于其还原性,与漂白性无关,C错误;浓硫酸能够使胆矾变白,这体现了浓硫酸的吸水性而不是脱水性,D错误。]
13.C [A对,SO2可使品红溶液褪色,①中棉花球颜色褪去;B对,KMnO4具有氧化性,能氧化SO2,②中棉花球颜色褪去,体现了SO2的还原性;C错,将生成的气体通入BaCl2溶液中发生反应:SO3+H2O===H2SO4,H2SO4+BaCl2===BaSO4↓+2HCl,由于H2SO3酸性小于HCl和H2SO4,因此SO2不能与BaCl2反应,故无BaSO3生成;D对,④为吸收尾气的装置,可发生反应:SO2+2NaOH===Na2SO3+H2O。]
14.D [纸浆漂白时留下的含氯物质具有强氧化性,硫代硫酸钠作脱氯剂时,主要利用其还原性,A项错误;“净化”时加入的试剂X是为了除去硫酸根离子,加入BaCl2溶液会引入新杂质氯离子不易除去,可选用Ba(OH)2溶液,B项错误;若pH过小,Na2S2O3不稳定,会发生歧化反应,使产率降低,C项错误;从溶液中获得的Na2S2O3·5H2O晶体中含有杂质,应先用水洗除去吸附的杂质离子,由于硫代硫酸钠晶体不溶于乙醇,再用乙醇洗涤除去水,D项正确。]
15.(1)Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
(2)将产生的气体通入品红溶液中,溶液褪色 (3)NaOH溶液 酸性氧化物 (4)2H++S2O===S↓+SO2↑+H2O
图片资源预览